تدریس ژنتیک : تدریس فصل چهاردهم (سرطان) ژنتیک پزشکی امری (ایمری) جلسه دوم
واژه سرطان به یک بیماری مجزا اطلاق نمی شود بلکه یک واژه عمومی برای تمامی نئوپلاسم های بدخیم است. زمانی به یک توده سلولی در حال تکثیر، بدخیم (Malignant) می گویند که مستقل از مکانیسم های کنترلی، رشد کند و توانایی عبور از مرزهای بافتی، رشد تهاجمی و ایجاد متاستاز را داشته باشند. برخی از انواع تومورهای بدخیم (برای مثال، کارسینومای سلول بازال) قدرت متاستازی پایینی دارند و ممکن است سال ها بدون ایجاد متاستاز رشد کنند. سه گروه اصلی از سرطان ها وجود دارند: کارسینوماها (Carcinomas)، که از بافت اپیتلیالی (مثل پوست، اپیتلیوم روده ای، اپیتلیوم تنفسی و اپیتلیوم مجاری غددی از قبیل غدد پستانی و پانکراس) ایجاد می شوند؛ سارکوماها (Sarcomas)، که از بافت مزانشیمی (مانند بافت پیوندی، استخوان ها، ماهیچه ها) منشا می گیرند؛ و بیماری های بدخیم سیستم های خونی و لنفاوی (به ترتیب، لوسمی ها Leukemia و لنفوم ها Lymphomas).
بیشتر انواع سرطان، بواسطه تجمع پیشرونده جهش های متنوع درون یک سلول ایجاد می شوند. این تغییرات ژنتیکی معمولا به صورت سوماتیکی کسب می شوند، اگرچه برخی از آنها می توانند از طریق رده زایا منتقل شوند و در لحظه تولد در همه سلول های بدن وجود داشته باشند. ژنهای مسئول پیشرفت سرطان در دو گروه اصلی دسته بندی می شوند: پروتوانکوژن ها و ژن های سرکوبگر تومور.
پروتوانکوژن ها: ژنهایی که بواسطه جهش های فعال کننده (غالب) می توانند به انکوژن ها تبدیل شوند. انکوژن ها ترانسفورماسیون بدخیم را از طریق سنتز پروتئین های تغییر یافته یا دارای ساختار معیوب تسهیل می کنند.
ژن های سرکوبگر تومور: ژنهایی که با فرایندهای تنظیم رشد، ترمیم و بقای سلولی که بواسطه جهش های حذف عملکرد (مغلوب) در هر دو نسخه ژن، دچار ترانسفورماسیون بدخیم شده است، مرتبط هستند. این ژن ها معمولا شامل ژن های ترمیمDNA هستند که مسئول شناسایی و ترمیم آسیب ژنتیکی درون سلول می باشند.
عملکرد هماهنگ بین ژن های افزایش دهنده و کنترل کننده رشد برای حفظ صحت عملکرد سلول های منفرد و گروه های بافتی مورد نیاز است. بروز سرطان، منعکس کننده از دست رفتن این سیستم بسیار متعادل است. جهش منفرد، هرگز موجب سرطان نمی شود، بلکه سرطان نتیجه تجمع تغییرات مختلف ژنتیکی و کروموزومی است. تنها پس از اینکه یک تعداد بحرانی از تغییرات ژنتیکی اتفاق می افتد، رشد کنترل شده اولیه تبدیل به یک رشد کنترل نشده بدخیم می گردد (ترانسفورماسیون بدخیم). گسترده ترین مطالعات در خصوص این موضوع بر روی سرطان کولورکتال انجام شده است. برت وگلشتاین و همکارانش مدل پیشرفت تومور Tumor progression model (توالی آدنوما کارسینوما) را شرح دادند. آنها با استفاده از این مدل توانستند تاثیر سلسله توالی نقایص ژنی مختلف بر روی ایجاد تومور را توضیح دهند. چگونگی ارتباط بین تجمع نقایص ژنتیکی در انکوژن ها یا ژن های سرکوبگرتومور و پارامترهای مورفولوژیکی قابل توجه است. پیشرفت تومور، از بافت طبیعی به آدنوما و کارسینومای کولون، حدود ۱۰ سال به طول می انجامد.
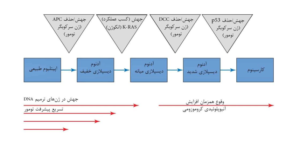
رشد کنترل نشده، مشخصه مشترک همه تومورها است چه تومورها بدخیم باشند چه خوش خیم. با این وجود، تومور های بدخیم توانایی رشد تهاجمی و ایجاد متاستاز را نیز دارند. رشد کنترل نشده تومور، حاصل اختلال در پردازش اطلاعات درون سلولی، و نیز بین سلولی است. بنابراین سرطان لزوماً نتیجه تکثیر سلولی افزایش یافته نیست. بلکه مربوط به مسئله تعادل بین تقسیم سلولی و رشد از یک طرف و آپوپتوز (مرگ سلولی برنامه ریزی شده) از طرف دیگر می باشد. موضوع اساسی برای تکوین رویانی، و نیز برای موجودات بالغ، این است که مسیرهای پیام رسانی متفاوت، بسیار هماهنگ و تنظیم یافته عمل کنند. بین درجه تمایز و میزان تکثیر یک سلول رابطه معکوس وجود دارد. تومور بدخیم نسبت به بافت منشا خود تمایل کمتری به تمایز یافتگی دارد.
انکوژن ها
.انکوژن ها بواسطه جهش های “هایپرمورفیک” که منجر به کسب عملکرد می شوند از پروتوانکوژن ها به وجود می آیند. چنین جهش هایی بیشتر جهش های بد معنی هستند که سبب فعال سازی دائمی یا عملکرد تغییر یافته محصول ژن (تغییرات کیفی) می-گردند. پروتوانکوژن ها همچنین می توانند دو برابر یا چند برابر (تکثیر) شوند که نتیجه آن، تعداد نسخه های افزایش یافته ژن و بنابراین محصولات ژنی بیشتر در سلول است. به علاوه، جابجایی ها می توانند پروتوانکوژن ها را از طریق تولید یک ژن همجوش با عملکرد جدید و/یا قرار دادن آن تحت کنترل پروموتر جدید و همیشه فعال، به یک انکوژن تبدیل نمایند، که ممکن است موجب بیان غیر طبیعی با توجه به سیستم اندام یا مرحله نموی شود.
غالب یا مغلوب؟. پروتوانکوژن های تیپیک در مسیرهایی دخالت دارند که رشد سلولی، تکثیر سلول و چرخه سلول را تنظیم می کنند. پروتوانکوژن ها شامل گیرنده های تیروزین کینازی، فاکتور های رشد و گیرنده های آنها، اجزای آبشارهای پیام رسانی درون سلولی و پروتئین های تنظیم کننده چرخه سلولی می باشند. انکوژن ها در سطح سلولی غالب هستند بدین معنی که فعال سازی یا بیان بیش از حد یک آلل منفرد برای ایجاد تغییر در فنوتیپ سلول کافی است.
دو مثال از انکوژن های گیرنده های تیروزین کینازیRET وMET هستند. RET گیرنده فاکتورهای رشد متعلق به خانواده فاکتور رشد مشتق از رده سلولی گلیال (GDNF) است. جهش های فعال کننده در ژن RET مسئول ایجاد MEN2، یکی از نئوپلازی های اندوکرین چندگانه هستند. نکته جالب توجه این است که جهش های غیر فعال کننده در همین ژن می تواند سبب بیماری هیرش اسپرانگ شود MET گیرنده فاکتور رشد کبدی (HGF) است. جهش در ژنRET می تواند منجر به کارسینومای کلیوی پاپیلاری خانوادگی گردد.
از میان فراوان ترین تغییرات انکوژنی می توان به جهش های ژن های خانواده RAS (مثل H-RAS، K-RAS، N-RAS) اشاره نمود. ژن های RAS، پروتئین های متصل شونده به گوانوزین تری فسفات (GTP) را کد می کنند که در آبشارهای پیام رسانی مهم مختلف در سلول به عنوان تنظیم کننده اصلی عمل می کنند. جهش های K-RAS در تقریبا ۹۰% از همه کارسینوماهای پانکراسی و ۵۰% از همه سرطان های کولون رخ می دهند ؛ جهش های N-RAS در ۳۰% از تمامی موارد AML اتفاق می افتند.
مثال کلاسیک جابجایی کروموزومی که منجر به فعال سازی پروتوانکوژن می شود جابجایی بین کروموزوم های ۹ و ۲۲ است که حاصل آن کروموزوم فیلادلفیا، t(9;22)(q34;q11)، است. در سطح مولکولی، جابجایی سبب همجوشی ژن های BCR و ABL می گردد
جابجایی های پروتوانکوژن ها به درون نواحی کروموزومی که تحت کنترل پروموتر ژن های زنجیره های ایمنوگلوبولین (کروموزوم-های ۱۴، ۲۲ و ۲) هستند، همانطور که در پروتوانکوژن MYC در لفنوم بورکیت مشاهده می شود موجب بیان دائمی و کنترل نشده آنها می گردند
| جابجاییهای کروموزومی به عنوان علل بیماریهای بدخیم | |||
| نئوپلازی | جابجایی | فراوانی | ژن همجوش یا انکوژن درگیر |
| CML (لوسمی میلوییک مزمن) | t(9;22)(q34;q11) | ۹۵%-۹۰% | BCR-ABL |
| ALL (لوسمی لنفاتیک حاد) | t(9;22)(q34;q11) | ۱۵%-۱۰% | BCR-ABL |
| لنفوم بورکیت | t(8;14)(q24;q32) | ۸۰% | MYC |
| t(8;22)(q24;q11) | ۱۵% | ||
| CLL (لوسمی لنفاتیک مزمن) | t(11;14)(q13;q32) | ۳۰%-۱۰% | BCL-1 |
| لنفوم فولیکولار | t(14;18)(q32;q21) | ۹۰%< | BCL-2 |
(تدریس ژنتیک)
مطالب مرتبط:
تدریس ژنتیک : تدریس فصل چهاردهم (سرطان) ژنتیک پزشکی امری (ایمری) جلسه اول
کارشناسی ارشد ژنتیک انسانی در یک نگاه، تعریف، رشته های مجاز، دروس و ضرایب، منابع، زمان آزمون ۹۷-۹۶
منابع مطالعاتی کنکور کارشناسی ارشد ژنتیک انسانی
کلاس های آمادگی کنکور کارشناسی ارشد ژنتیک انسانی
در پایان به دانشجویانی که تمایل دارند از مباحثی که از ژنتیک پزشکی ایمری در کانال ژنتیک پزشکی متعلق به همین سایت تدریس می شود استفاده کنند پیشنهاد می گردد از طریق این لینک به کانال ژنتیک پزشکی بپیوندند.